Pressemitteilung der Universität Duisburg-Essen
Wie der Wirt Bakterien erkennt
[20.07.2012] Bakterien, Viren, Pilze und Parasiten umgeben uns. Dass wir trotzdem nicht krank werden, liegt an bestimmten zellulären Sensoren, wie den Toll-like Rezeptoren (TLR). Sie erkennen molekulare Muster von Erregern und leiten ihre meist völlig unbemerkte Vernichtung ein. Diese immunaktivierenden Fähigkeiten wurden erst 1998 entdeckt, dafür gab es den Nobelpreis. Jetzt untersuchte ein internationales Forscherteam um Prof. Dr. Carsten Kirschning vom Institut für Medizinische Mikrobiologie des Universitätsklinikums Essen und der Universität Duisburg-Essen (UDE) sowie Privatdozent Dr. Hubertus Hochrein die komplexe Erkennung von Bakterien. Die Ergebnisse sind im Wissenschaftsmagazin Science nachzulesen.
Unser angeborenes Immunsystem ist klug. Bestimmte Strukturen, die charakteristisch für viele Mikroorganismen sind, erkennt es und schlägt Alarm. Toll-like Rezeptoren lösen dann die wichtige Entzündungsreaktion aus. Das kann aber auch gefährlich werden: Weil TLR so empfindlich sind, kommt es bei schweren Infektionen zum Überschießen der Immunantwort. Die Folge: Blutvergiftung und oftmals ein septischer Schock.
Deshalb nahmen die Experten die Wirtserkennung von Staphylokokken- und E.coli-Bakterien, die häufig Blutvergiftungen auslösen, unter die Lupe: Sie konnten nachweisen, dass TLR13 ein spezifisches Segment der bakteriellen ribosomalen Ribonukleinsäure erkennt. Daran binden sich auch spezifische Antibiotika wie z.B. Erythromycin, falls das Segment nicht wie bei resistenten Erregern verändert ist. Die konkrete Ribonukleinsäure wird als 23S rRNA bezeichnet. „Tierische und menschliche Ribosomen binden Erythromycin hingegen nicht an ihre 28S rRNA, weil ihre Struktur diesbezüglich der 23S rRNA resistenter Bakterien ähnelt“, erklärt Prof. Dr. Carsten Kirschning.
Bedeutsam sind die neuen Erkenntnisse für die Behandlung bakterieller Infektionen und das Verständnis von Antibiotika-Resistenzen. Außerdem könnten sie bei der Therapie von immunologischen Überreaktionen helfen und neue Impfstrategien eröffnen.
Die Studie stammt von einem internationalen Forscherteam um Prof. Dr. Carsten Kirschning vom Institut für Medizinische Mikrobiologie des Universitätsklinikums Essen und der UDE, Privatdozent Dr. Hubertus Hochrein von der Firma Bavarian Nordic GmbH in Martinsried, Prof. Dr. Stefan Bauer vom Institut für Immunologie der Phillips-Universität Marburg und Prof. Dr. Hermann Wagner vom Institut für Medizinische Mikrobiologie, Immunologie und Hygiene der Technischen Universität München. Dazu gehören weitere Wissenschaftler aus München, der Schweiz und Japan.
Die Publikation ist hier online abrufbar: http://www.sciencemag.org/cgi/content/abstract/science.1220363
Weitere Informationen:
● Prof. Dr. Carsten Kirschning, Tel. 0201/723-1824, Mobil: 01609/254-7309, carsten.kirschning@uk-essen.de
● Pressesprecherin des Universitätsklinikums Essen: Christine Harrell, Tel. 0201/723-3107, christine.harrell@uk-essen.de
Redaktion: Carmen Tomlik, Tel. 0203/379-1489
Bildhinweis:
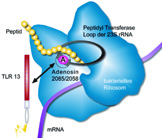
Ein Foto zu dieser Pressemitteilung (Bildbeschreibung: Ein spezifisches Segment der bakteriellen 23S ribososmalen (r) RNA aktiviert den Toll-like Rezeptor 13. Es ist bereits bekannt, dass dieses 23S rRNA-Segment Antibiotika wie Erythromycin bindet. Sein zentrales Adenosin (A) 2085 in S. aureus und A2058 in E. coli 23S rRNA ist in Erythromycin-resistenten Bakterien mutiert oder methyliert. Bilddesign: Daniela Willemsen
) können Sie herunterladen unter:
"http://www.uni-due.de/imperia/md/images/samples/2012/bilderpressemitteilungen/tlr13_bindet_bakt._23s_rrna_korr.jpg.jpg"
Alle Pressemitteilungen der UDE finden Sie unter:
http://www.uni-due.de/de/presse/pm.php
